James Allison perdió a su madre apenas cuando apenas él tenía 11 años. Después murió su hermano y dos de sus tíos. El cáncer se los había llevado por delante. Reconoce que fue motivación suficiente para ponerse a indagar sobre tumores que, sin embargo, nunca ha tenido interés en combatir directamente. Ahora, décadas después, ha podido conocer a pacientes que le deben la vida. No es médico. Hace investigación básica en biología.
Allison está detrás del trabajo previo hasta conseguir algunas de las medicinas más esperanzadoras contra el cáncer. Tratamientos que, paradójicamente, no actúan sobre tumor alguno. Allison es el padre de la inmunoterapia de alta eficacia: cuando es nuestro propio organismo el que combate la enfermedad. Una verdadera batalla de robocops dentro del organismo, como ilustramos en este vídeo:
Así funciona una batalla contra células malignas por parte de los robocops del organismo: las células T (CTL / CD8). Y así trabaja el doctor Allison, al que descubrimos tocando la armónica con su grupo de música country. | Vídeo: M. Viciosa, Nature, Fundación BBVA
Allison acaba de ser galardonado con el Premio Fronteras del Conocimiento de la Fundación BBVA en Biomedicina. Junto a su equipo, en el que destaca su mujer, la doctora Padmanee Sharma, dirige el Departamento de Inmunología de la Universidad de Texas-Austin / MD Anderson Cancer Center. Desde los años noventa, han buscado la manera de resucitar la inmunoterapia, relativamente abandonada después de que en los años setenta diera buenos resultados en ratones, pero no en humanos.
Cuando todo parecía fallar
“Algo fallaba, se iba a ciegas, no se había hecho el trabajo de ciencia básica”, recuerda Allison en conexión desde California (EE.UU.) tras anunciársele el premio. Se dieron cuenta de que se podía estimular el sistema inmunitario y, en particular, los llamados linfocitos T (CLT o CD8) para que atacasen a las células tumorales. Esos linfocitos son como los robocops de la policía. Intervienen en el cuerpo a cuerpo y en primera línea de ataque contra las malignas células atrincheradas en un tumor. Por supuesto, sólo actúan al recibir una serie de señales. En el caso del organismo, señales químicas.
Sin embargo, en un momento dado, se dieron cuenta de que esas brigadas se retiraban. ¿Qué las frenaba? A finales de los ochenta se descubrió una molécula en su superficie: CTLA-4. Es decir, el pedal de freno de las células T, los robocops. Las células tumorales habían, de alguna manera, aprendido a usarlo a su favor.
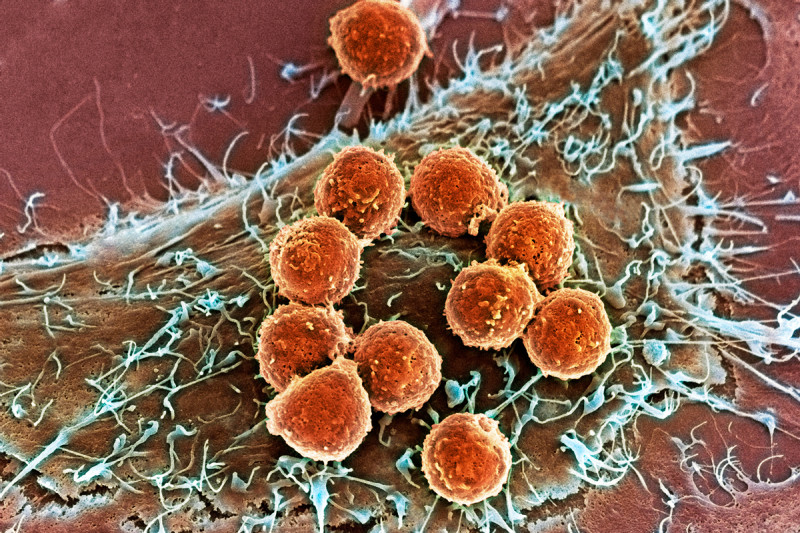
Células T (naranjas) atacando un tumor
La cuestión era que no se puede eliminar ese freno porque las T podrían empezar a matar células a discreción, cargándose también a las sanas. Eso es lo que solemos entender como enfermedad autoinmune.
Se encontró la manera de controlar el pedal de freno de las defensas
Allison encontró la manera de controlar ese pedal de freno, para que no se pare del todo la acción de las células T contra los tumores. Inhibiendo la molécula CTLA-4, consiguió el desarrollo del primer medicamento aprobado en 2011 en Estados Unidos contra el melanoma avanzado: ipilimumab. Junto al nivolumab (un medicamento que impide a las células T apagar su interruptor PD-1), “permite ahorrar sesiones de quimio y radioterapia”, añade Allison.
Estas investigaciones han dado vida a una veintena de medicamentos “contra los cánceres de riñón, cabeza y cuello, vejiga y pulmón”, aunque “no funciona en otros, hay todavía mucho trabajo. Es cierto que no vamos a curar todos los tipos de cáncer, pero creo que la inmunoterapia formará parte del arsenal terapéutico contra muchos tumores”. Moderado optimismo de Allison que concreta en una cifra: “entre el 60% y 90% de los casos en ciertos tipos de cáncer [se curará así]. Con este enfoque se pueden abordar mutaciones heterogéneas. Tumores no provocados por carcinógenos no específicos".
Hoy, decenas de científicos de todo el mundo vuelven a centrar sus esfuerzos en el desarrollo de medicamentos y en la búsqueda de palancas que activen y desactiven defensas contra los tumores. En Madrid, el año pasado investigadores del Hospital Gregorio Marañón y de la CUN presentaron un fármaco que se inyecta directamente en los tumores sólidos de mal pronóstico. En fase experimental, la sustancia desarrollada en España simula un virus, que logra una respuesta antitumoral directa y activa las defensas contra las células malignas.
Así pueden ser las inmunoterapias hoy
- Interferones: lucha contra el invasor: Tratamiento probado para el melanoma y la leucemia mieloide crónica. Son agentes normalmente liberados por leucocitos contra los elementos invasores.
- Interleucinas: proteínas para ‘muscular’ las defensas: Son una especie de alimento para las células inmunitarias, les hace crecer y ser más activas. Una de ellas se usa contra cánceres renales y melanomas con metástasis.
- Anticuerpos monoclonales: operarios de palancas en las células: Como se puede ver en el vídeo, son una especie de híbridos de células mezcladas que actúan sobre la superficie de las células defensoras y tumorales. Activan y desactivan respuestas de unas sobre otras. Son prometedores como tratamiento y útiles en el diagnóstico.
- Vacunas: presentarle el cáncer al organismo: como toda vacuna, se trata de introducir en el cuerpo un patógeno desactivado para que éste lo reconozca y, en su caso, genere anticuerpos. En el caso del cáncer, se pueden usar células malignas que ya no se pueden reproducir o usar antígenos que se unen a células cancerosas. Recientemente, se ha conseguido que las defensas que han conocido un tumor puedan "buscar" en casi todo el organismo restos cancerosos y atacarlos.
- Estimulantes del colonias: crear legiones de defensores: Los CSF actúan en la médula ósea, que es donde nacen leucocitos, eritrocitos y plaquetas. Se trata de que, sencillamente, haya más, para lo que se favorece la división celular de estos agentes de las defensas.
El científico que conoce a quien salvó la vida
No es habitual que un científico básico conozca aplicaciones concretas y cotidianas de sus descubrimientos. Menos aún, en medicina, que se encuentre con pacientes que han sobrevivido a tumores considerados mortales de necesidad. "He visto pacientes que han sobrevivido. Una veinteañera –recuerda Allison– que acababa de terminar sus estudios y se iba a casar me fue presentada por sus oncólogos. Han pasado 13 años de aquello, ahora tiene dos hijos. Es una persona con una vida plena".
Otro caso fue el de una paciente diagnosticada en 2001. "Todo había fracasado. Le dijeron que le quedaban dos meses de vida. Probó con el ensayo clínico. Hoy, su hijo sé que se va a a graduar en secundaria. Estoy hablando de más de diez años más después del acabar el tratamiento", destaca Allison.
He conocido a una paciente tratada con inmunoterapia a la que habían dado dos meses de vida hace más de 10 años
"El melanoma era muy mortal, se daban unos 11 meses de vida al paciente. Por eso empezamos [a investigar] con él. Ahora, el 60 % sobrevive con terapia combinada". De la segunda generación de medicamentos, los anti PD-1, hay cuatro aprobados en Estados Unidos para diferentes tipos de cáncer.
"La mayor parte de los oncólogos dicen que si queda un puntito de cáncer, puede reactivarse, pero los pacientes recuperados que he conocido ya no se preocupan porque tienen la seguridad de que eso no ocurrirá". Para Allison, la mayor recompenses "es ver a la gente libre de enfermedad después de todo ese tiempo, diez años o más, hacen una vida normal. No van a morir por esa enfermedad".
Por supuesto, no todo es de color de rosa. "No sabemos por qué no funciona en todos los pacientes; hay muchas personas investigando esta cuestión, buscando marcadores o señales para predecir quién va a responder al tratamiento y quién no". Por otro lado, "cánceres como el mioblastoma o el de páncreas no responden por el momento" a la inmunoterapia. Tan crudo como esperanzador. "Soy optimista, pero es sólo el comienzo".
Te puede interesar
Lo más visto




