Los seres vivos tenemos ritmos biológicos que regulan nuestra actividad, desde el sueño al hambre, con la producción de ciertas hormonas. Ahora, un grupo de investigadores del Centro Nacional de Investigaciones Cardiovasculares (CNIC) ha descubierto que las defensas también tienen ciclos circadianos y cómo estos pueden ayudar a luchar contra algunas de las enfermedades más graves en la actualidad, ictus, enfermedades cardiovasculares o procesos inflamatorios agudos, además de infecciones.
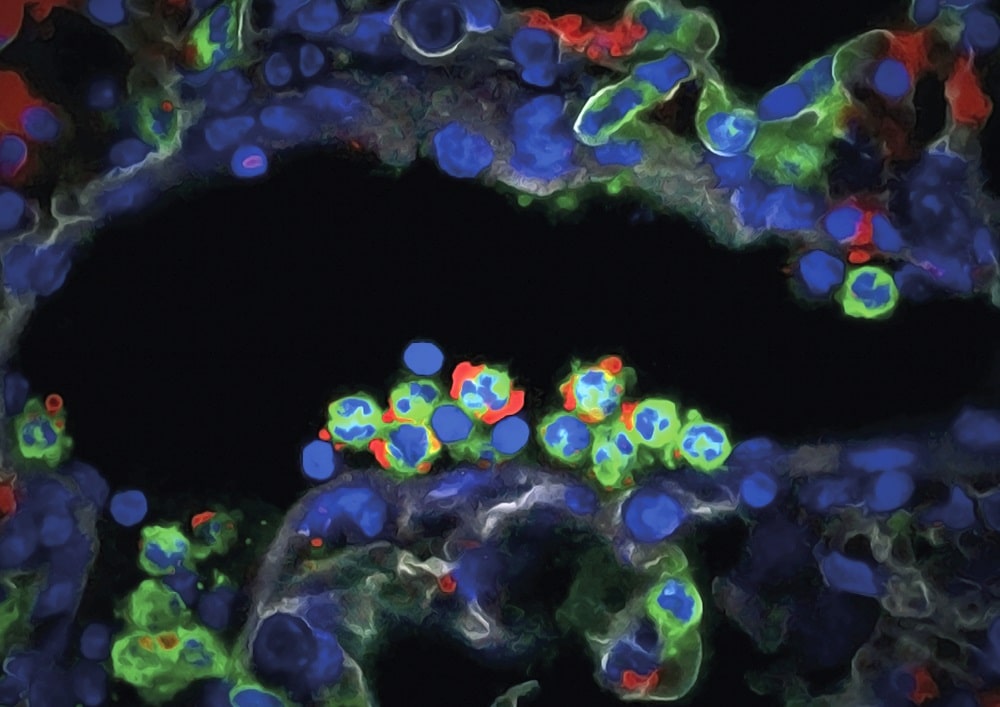
La clave del hallazgo, que se publica en Nature Inmunology está en las células más abundantes del sistema inmune, los neutrófilos, que son las primeras en responder ante los ataques externos. Los investigadores han descubierto que los neutrófilos siguen un ciclo circadiano (que dura, como sugiere su nombre, aproximadamente un día) que se relaciona con su capacidad para responder a las agresiones externas con mayor o menor virulencia. Además, han comprobado en ratones que este ciclo puede ser modificado y con éste su respuesta del cuerpo ante distintas enfermedades o infecciones.
Estas células son las primeras que llegan al foco infeccioso inflamatorio para eliminar las agresiones pero son muy destructoras y, si se activan en un momento inadecuado, pueden dañar tejidos sanos. De hecho, esa falta de regulación de los ataques está detrás de muchas enfermedades autoinmunes o neurodegenerativas. "Estas células tienen en su interior unos gránulos que son los que almacenan el 'arsenal' de sustancias tóxicas contra las agresiones. Lo que hemos descubierto es que a lo largo del día, las células se van deshaciendo de ese arsenal y resultan menos tóxicas", afirma Andrés Hidalgo, uno de los autores del estudio.
Ese 'desarme', que evita también que estas células puedan dañar tejidos sanos, explica cómo hay muchas enfermedades que dañan más o menos si ocurren de día o de noche, tal como los investigadores han podido comprobar respecto a los ictus. "Los ictus ocurren por la mañana con más frecuencia y, además, son más severos a esa hora", apunta Hidalgo. El trabajo ha combinado la experimentación en ratones con el cruce con datos de pacientes del Hospital Clínic de Barcelona que habían sufrido procesos de inflamación aguda de pulmón.
“Una vez que hemos aprendido cómo funciona este proceso de manera natural, lo que podemos hacer es tratar de controlarlo para obtener un beneficio clínico”, asegura Alejandra Aroca, coautora del estudio. “Esto ya lo estamos intentando y hemos obtenido resultados prometedores en modelos preclínicos de infarto agudo”.
En los trabajos realizados con ratones para modificar ese ciclo ha obtenido resultados prometedores, como explica Hidalgo. "En daño pulmonar, modificando al máximo posible los gránulos del interior de los neutrófilos conseguimos reducir el 90% la severidad del daño en el tejido y hasta un 50% las muertes relacionadas. Además, la modificación no dejaba a los ratones especialmente desprotegidos contra las infecciones", añade el investigador.
Y es que la clave, explica Hidalgo, es encontrar el 'switch point' o punto clave en el que se equilibra la respuesta inmune. Esto nos abre la puerta a regular la respuesta a enfermedades cardiovasculares como infartos, embolias, inflamaciones agudas de pulmón o ictus, además de infecciones si regulamos las células en el otro sentido".
Te puede interesar
-
Quirónsalud impulsa su plan de sostenibilidad con menos emisiones y mayor eficiencia energética
-
El aviso del doctor Rahmstorf sobre la mancha fría del Atlántico que solo Islandia ha escuchado
-
Este es el plazo que da la ciencia para la llegada de un gran tsunami al Mediterráneo
-
El tiempo en la Tierra está cambiando: ¿estamos de camino a los días de 25 horas?
Lo más visto