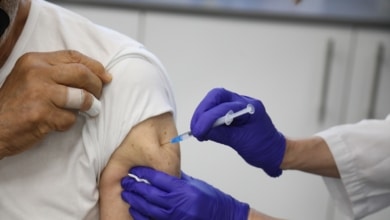
La Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha aprobado este viernes la administración de la vacuna contra el Covid-19 Spikevax (anteriormente llamada Moderna) en niños de 12 a 17 años en la Unión Europea. Este fármaco ya estaba autorizado para mayores de 18 años.
Se administrarán dos inyecciones con cuatro semanas de diferencia. Los efectos de Spikevax se han investigado en un estudio en el que participaron 3.732 niños de esas edades. La investigación, según ha explicado la EMA en un comunicado, se está llevando a cabo de acuerdo con el plan de investigación pediátrica (PIP) de Spikevax, que fue acordado por el Comité Pediátrico de la EMA (PDCO).
El estudio ha mostrado que Spikevax produjo una respuesta de anticuerpos en jóvenes de 12 a 17 años comparable a la observada en adultos de 18 a 25 años. Además, ninguno de los 2.163 niños que recibieron la vacuna se infectó de Covid-19, en comparación con cuatro de los 1.073 niños que recibieron una inyección ficticia. Por todo ello, la EMA concluye que la eficacia de Spikevax en jóvenes de 12 a 17 años es similar a la de los adultos.
Los efectos secundarios más comunes en los niños de 12 a 17 años son similares a los de las personas de 18 años o más, entre los que se encuentran dolor e hinchazón en el lugar de la inyección, cansancio, dolor de cabeza, dolor muscular y articular, agrandamiento de los ganglios linfáticos, escalofríos, náuseas, vómitos y fiebre. Estos efectos suelen ser leves o moderados y mejoran a los pocos días de la vacunación, indican.
La EMA sostiene que seguridad y eficacia de la vacuna tanto en niños como en adultos continuará siendo monitoreada de cerca, ya que se utiliza en campañas de vacunación en los Estados miembros del grupo comunitario, a través del sistema de farmacovigilancia de la UE y los estudios en curso y adicionales de la empresa y las autoridades europeas.
Te puede interesar
Lo más visto