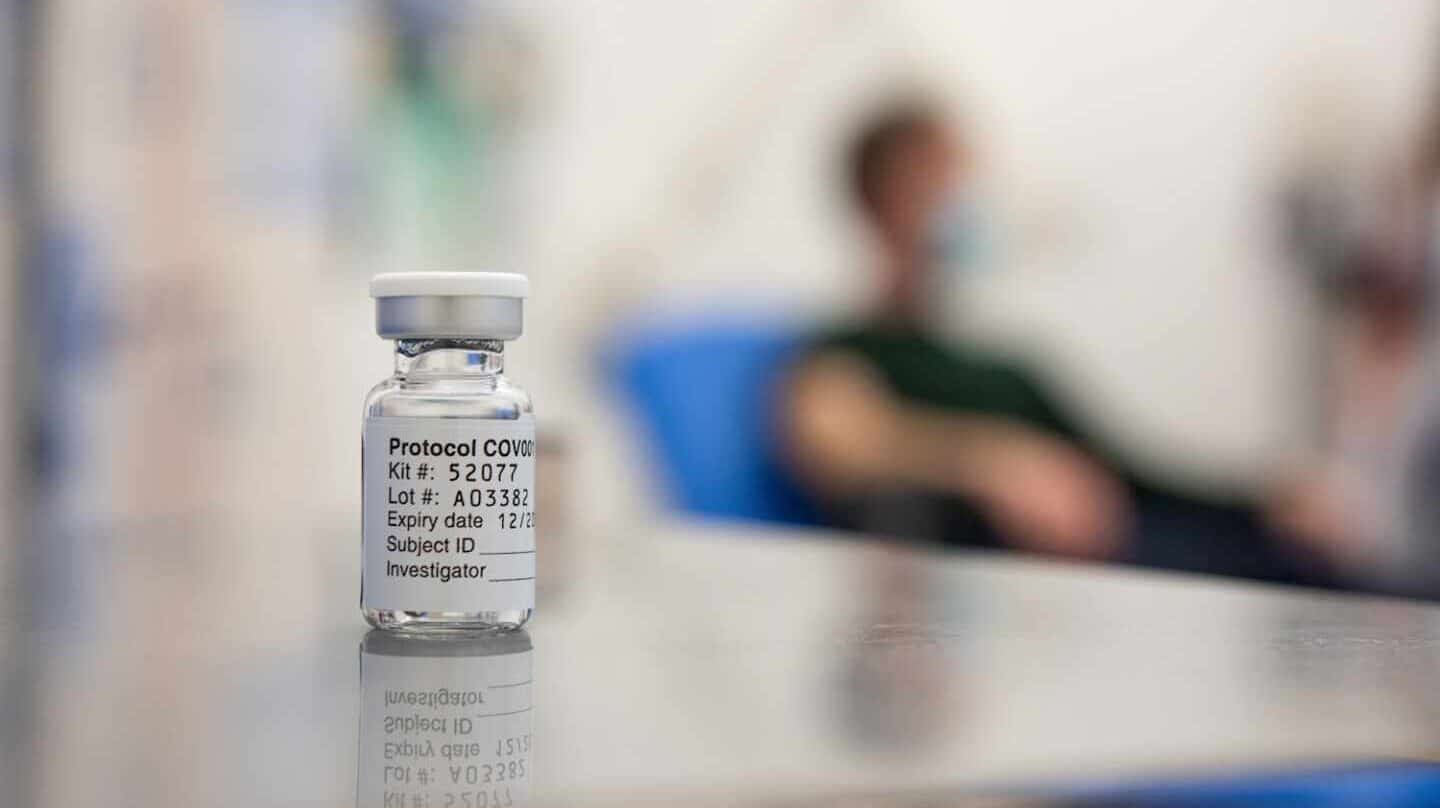
Nunca la ciencia ha estado tan pegada a la gente como en la pandemia de coronavirus. La carrera por la vacuna - que ya se compara con la carrera espacial - es uno de los espectáculos científicos que estamos viviendo en directo en esta crisis sanitaria. En los últimos diez meses hemos visto avances, acuerdos, efectos secundarios y subidas bursátiles de las compañías que iban despuntando con sus proyectos de inmunización. En contrapartida, hemos ido conociendo las reticencias de la población a vacunarse por la desconfianza en unas vacunas que prometen reducir a una décima parte los tiempos habituales de desarrollo.
"Una vacuna tarda en desarrollarse entre cinco y diez años aunque algunas como la del VIH llevamos 30 años buscándola sin éxito. Lo que hemos conseguido era impensable pero se ha conseguido sin atajos, sin poner en juego la seguridad", reconoce Mariano Esteban, investigador y responsable de uno de los proyectos de vacuna contra el Covid en el Centro Superior de Investigaciones Científicas (CSIC).
Hasta ahora, la inmunización que se había conseguido en menos tiempo fue la del ébola, lograda en cinco años. "Esto es una situación excepcional y se esperan también soluciones excepcionales. No se ha saltado ningún paso, pero se ha optimizado cada uno de ellos, se han acelerado los aspectos más burocráticos y engorrosos y, sobre todo, se han simultaneado pasos", explica el investigador Federico Martinón, experto en vacunología infantil.
Los pasos en el desarrollo de una vacuna
Conseguir una vacuna desde cero empieza con el descubrimiento de la molécula y de la plataforma vacunal. "Cuando se obtiene, se hacen unos pocos lotes para caracterizar y optimizar la producción de la vacuna, su estabilidad, si la formulación es correcta, su caducidad... Tras ello se ve si cumplen las buenas prácticas de producción, garantías de calidad y reproducibilidad [capacidad de ser reproducido igual a gran escala], que son muy estrictas por tratarse de medicamentos biológicos", explica Alejandro Orrico, farmacéutico e investigador en el área de vacunas de la Fundación para el Fomento de la Investigación Sanitaria y Biomédica de la Comunitat Valenciana (Fisabio).
Esos pasos, en los que habitualmente ya se ha consumido más de un año, preceden a los ensayos preclínicos in vitro (en tejidos) y con animales, en los que se estudia la inmunogenicidad o capacidad de generar reacciones del sistema inmunitario. "Eso no se hace en una sino en varias especies. Primero habitualmente en ratones y no en ratones cualquiera, muchas veces se necesita que sean humanizados, modificados genéticamente, y son caros y no fáciles de encontrar, especialmente este año cuando todo el mundo los necesitaba. Después se trabaja con otros animales, como monos, que tampoco es sencillo ni todos los laboratorios están preparados", continúa Orrico.
Algún año más pasa antes de que la vacuna pueda estudiarse en humanos, como explica el investigador de Fisabio. "Antes de empezar los estudios clínicos deben tener la aprobación de un comité de ética y de la agencia del medicamento. Y ahí es otro laboratorio el que suele coordinar el ensayo. Ponerlo en marcha lleva meses".
La tasa de éxito de las vacunas es muy pequeña, en torno al 5 o 6%. El resto nunca llega a comercializarse"
Los ensayos en humanos tienen necesariamente tres fases para estudiar su seguridad y eficacia. En condiciones normales, sólo cuando una de ellas ha acabado se evalúan los datos "y se valora si merece la pena seguir invirtiendo dinero, lo que no siempre es así, la tasa de éxito de las vacunas es muy pequeña, en torno al 5 o 6%. El resto nunca llega a comercializarse", indica Orrico.
Tras finalizar los ensayos, prepara la documentación para la solicitud de aprobación por parte del agente regulador y cuando esta llega, "se empieza a consistencia de lotes, para confirmar la capacidad de fabricación a gran escala. Después se fabrica y, al final, llega al canal de comercialización", añade Martinón.
¿Cómo ha sido posible reducir tanto los tiempos?
Para Esteban, tres factores han pesado para lograr este hito de la vacunación que supondrá - si se cumplen las actuales previsiones - que Europa y EEUU puedan empezar a vacunar a su población un año después del estallido de la epidemia. "Se ha unido el impacto de la pandemia en la economía global, con las cantidades ingentes de dinero inyectadas para conseguirlo y una infraestructura científica potente y muy desarrollada".
Coincide Orrico en que se ha mezclado "una inversión sin precedentes, en muchos casos a riesgo, con el conocimiento científico de miles de laboratorios del mundo trabajando al mismo tiempo y una red de colaboración sin igual".
Vacunas estándar vs vacunas del Covid (EMA)
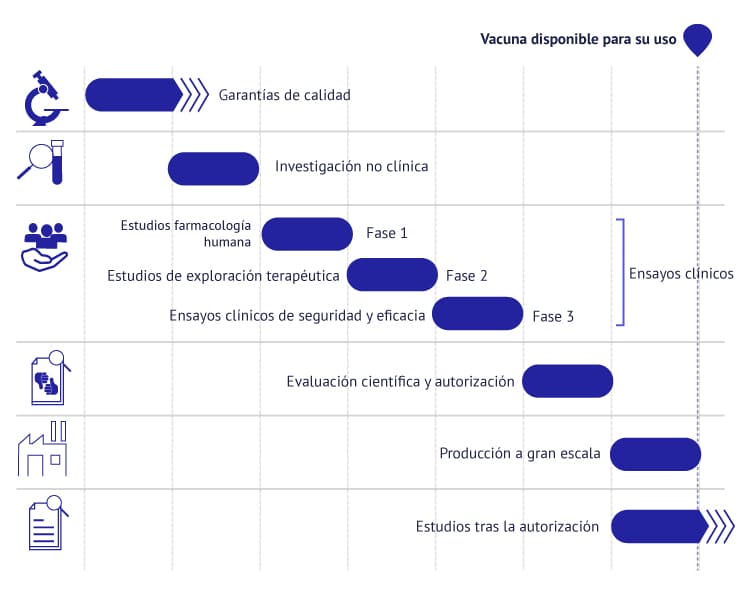
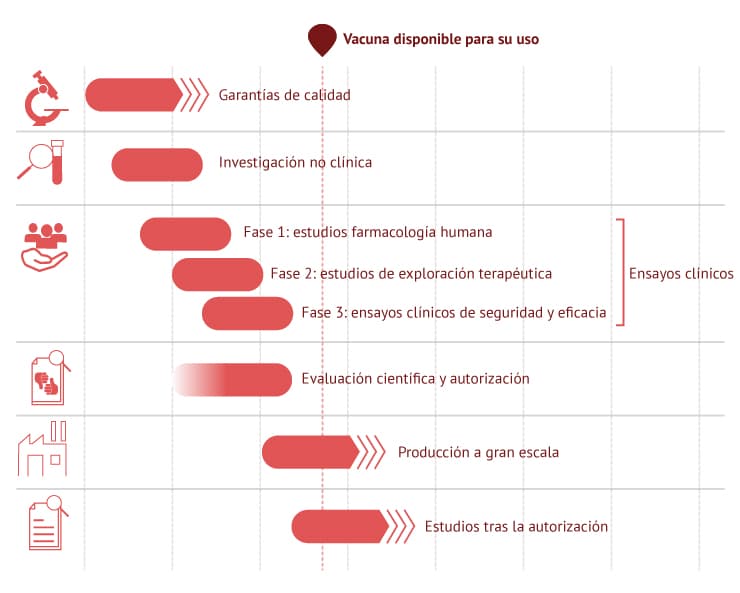
"Los Estados han puesto dinero a fondo perdido. El proyecto Covax en la Organización Mundial de la Salud (OMS) o el WRAP en Estados Unidos han sido fundamentales para permitir que las empresas, sobre todo algunas más pequeñas como Moderna, entraran en esta carrera", afirma Martinón. "Mientras que Pfizer ensayaba la vacuna ya había hecho el proceso de consistencia de lotes e incluso se estaba empaquetando. Con el riesgo de que si esta vacuna nunca sale, millones de dosis se irán por el fregadero", añade.
Mientras que Martinón afirma que el coste medio estimado para el desarrollo de la vacuna es de un billón de euros, "Pfizer ya ha asegurado que lleva invertidos 2,5 billones. La diferencia es notable y a veces el desarrollo de vacunas no va más rápido por falta de conocimientos sino de recursos. Y es que en otras vacunas no es que no se pueda, es que ni se intenta, porque no hay la necesidad ni la demanda, ni se asumen todos los riesgos de golpe".
Tras la inversión, otro de los aspectos decisivos ha sido el desarrollo de las fases en paralelo. "Ninguna fase se ha eliminado o se ha saltado algún paso, sólo se ha eliminado la burocracia y se han desarrollado en paralelo. Las fases de ensayos clínicos se han realizado de una manera simultánea", explica Orrico.
El último, que ninguna de las dificultades de las que se hablaba - capacidad para encontrar animales de experimentación o de empresas que elaboren componentes necesarios para el proceso se ha dado en esta ocasión. "Todo el mundo trabajaba al unísono, se ha colaborado entre empresas de todo el mundo", indica el investigador del CSIC.
Fast track de las agencias reguladoras
En cuanto al papel de las agencias reguladoras, los científicos preguntados por El Independiente coinciden en que "en ningún momento habrá un trato de favor con estas vacunas. La FDA o la EMA tienen una serie de prerrequisitos ya establecidos. Si se cumplen, se entra. Si no, no", asegura Martinón.
Sin embargo, Martinón puntualiza que la pandemia de Covid ha entrado en las agencias por un canal especial: "Los reguladores ya contemplan lo que se denominan procesos acelerados para situaciones de urgencia. Es lo que se denomina fast track en Europa y supone que los procesos de aprobación de datos son mucho más ágiles: Lo que en condiciones normales tarda un mes se consigue de un día para otro. Obviamente esto no puede hacerse así con todos los fármacos porque se colapsaría el sistema, pero ha supuesto un importante ahorro de tiempo".
Además, como explica Esteban, no será cuando los proyectos vacunales terminen los ensayos en fase 3 cuando las reguladoras tengan que empezar a analizar los datos para su aprobación. "En la pandemia, las compañías han ido manteniendo un contacto con los reguladores durante todo el proceso. La información se ha ido transmitiendo y eso posibilitará que una vez acaben los ensayos se puedan autorizar en muy poco tiempo".

Efectos secundarios y datos en directo
El anuncio de la paralización de ensayos clínicos - que se dio en dos de las vacunas hace algunas semanas - o las noticias como la que trascendía esta semana de que en uno de los grupos de ensayo de la vacuna de Oxford no había mayores de 55 años no son, para Federico Martinón, situaciones extrañas al proceso de desarrollo de una vacuna: "Vivimos un exceso de comunicación, estamos viendo en directo la transmisión del desarrollo clínico de las vacunas, es como si estuviéramos retransmitiendo en directo una operación a corazón abierto y la audiciencia fuera interpretando lo que están haciendo en cada momento y dictando lo que deberían hacer. Y qué rojo está eso, yo eso lo apartaría, le tiembla la mano al ciurujano… Es normal que la gente piense así incluso cuando lo hacen algunos sanitarios pero los que llevamos años trabajando en vacunas vemos que son situaciones normales, que denotan que el proceso se lleva a cabo de forma segura".
Así, el científico resta importancia a estas noticias y fija el foco en los dictámenes de las agencias reguladoras. "Son pasos intermedios, se hacen públicas cosas que normalmente no trascienden y para las que la población no tiene los elementos de juicio necesarios. Los que tienen que hablar son los reguladores y ellos dirán si la vacuna sale adelante o no".
Esa información llegará, si todo funciona como se espera, a principios de 2021. Esteban cree que la vacuna podrá comenzar en esas fechas "siempre con los grupos prioritarios porque no habrá para todos, y con unos requisitos importantes de seguimiento".
En ese seguimiento estará muy de cerca el área de Fisabio en que trabaja Orrico, que ya está involucrado en la preparación de los procesos que supondrán la fase 4 del ensayo de las vacunas del Covid. "Nosotros somos parte del sistema de farmacovigilancia que ya se está desarrollando para cuando la población comience a vacunarse. Ya están preparados los protocolos de cómo deben reportarse y organizarse por edades las posibles incidencias y también se están estableciendo las incidencias de salud más probables que pudieran darse con las vacunas para poder compararlas con las que se produzcan tras la vacunación", explica el investigador valenciano.
Un desarrollo sin precedentes que Esteban espera no vuelva a sorprender a España. "Se ha visto que cuando se quiere puede y que el desarrollo de los países está supeditado a su capacidad para generar conocimientos. Que es necesario un sistema científico y empresarial robusto para evitar debilidades frente a otra pandemia. Se ha visto también la vulnerabilidad de la sociedad en su conjunto, que no sirve de nada protegerse a uno mismo si el vecino no lo está. Hay una importante enseñanza de que la emergencia es global y así debe abordarse", concluye.
Te puede interesar
Lo más visto