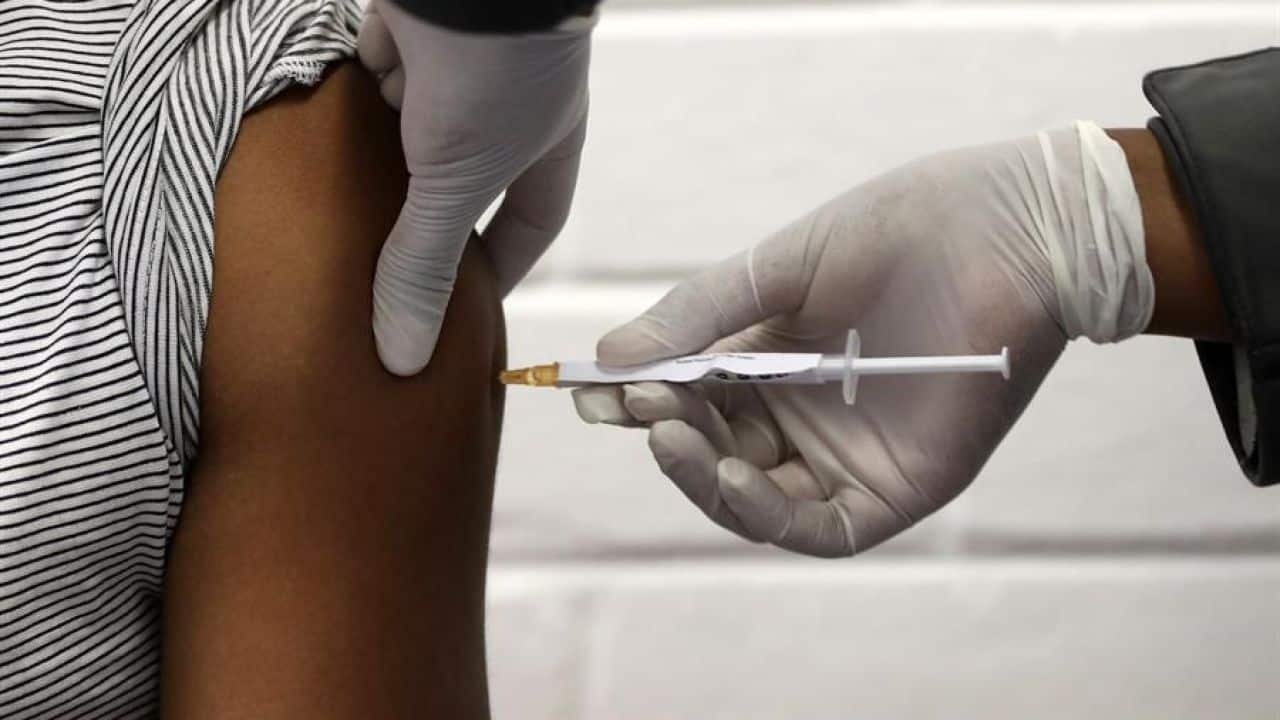
La empresa biomédica Moderna ha anunciado este lunes que su candidata a convertirse en la primera vacuna contra el Covid-19, ARNm-1273, tiene una eficacia del 94,5%, un porcentaje superior al 90% que comunicó la compañía Pfizer hace una semana.Este primer análisis provisional ha contado con la participación de 95 pacientes infectados por Covid-19.
Este primer análisis provisional ha contado con la participación de 95 pacientes infectados por Covid-19 y en las próximas semanas, Moderna solicitará a la Administración de Medicamentos y Alimentos (FDA) de EEUU una Autorización de Uso de Emergencia que se basará en el análisis final de 151 casos, los cuales han contado con un seguimiento sanitario de dos meses.
La empresa ha añadido que su vacuna candidata cuenta con un periodo más extenso de conservación en estado de refrigeración. Además, este antídoto podrá mantenerse a una temperatura de 20 grados bajo cero por un periodo de seis meses, es decir, 50 grados más alto que la de Pfizer, por lo que será más óptima de cara a exportarse y almacenarse a largo plazo. La compañía ha destacado que su fármaco tiene la capacidad de mantenerse estable en temperaturas entre 2° y 8°C por un periodo de 30 días.
El pasado viernes, Moderna afirmó que había completado la acumulación de datos para un primer análisis de su vacuna, aunque, para que los ensayos de los fármacos progresasen a buen ritmo hacía falta que los voluntarios se infectasen, según explicaron en un comunicado de prensa.
Moderna ha experimentado un aumento significativo en la tasa de identificación de casos durante la última semana. El 22 de octubre, el estudio completó la inscripción de 30.000 participantes en Estados Unidos, en el que se incluyó a más de 7.000 personas mayores de 65 años y a otros más de 5.000 menores de 65 años con alto riesgo enfermedades crónicas, como diabetes, obesidad grave y enfermedades cardíacas.
Te puede interesar
Lo más visto