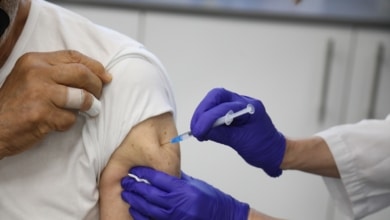
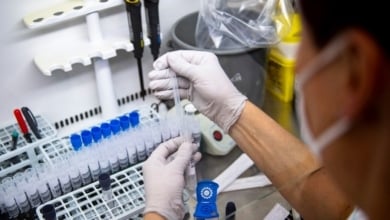
Uno de los problemas que el Covid ha dado a los médicos e investigadores de todo el mundo ha sido su capacidad para infectar células de otros órganos más allá del aparato respiratorio y que hacía imprevisible averiguar quiénes iban a empeorar. Su virulencia sobre el sistema inmunológico y la hiperinflamación que genera pueden hacer más daño que el propio virus a personas con enfermedades previas muy distintas. Obesidad, diabetes, EPOC o tener edad avanzada son condicionantes de riesgo para el Covid cuya asignatura pendiente siguen siendo los tratamientos un año después del estallido de la pandemia.
Por eso la importancia de cada nuevo hallazgo para hacer frente a la enfermedad y especialmente cuando ataca el campo con menos opciones disponibles, cuando la enfermedad es aún leve. En este contexto se encuentran dos anticuerpos monoclonales (bamlanivimab y etesevimab) que la Agencia Europea de Medicamentos acaba de avalar a través de una recomendación previa. Es la antesala de su autorización definitiva pero permite ya su uso de emergencia en los países europeos.
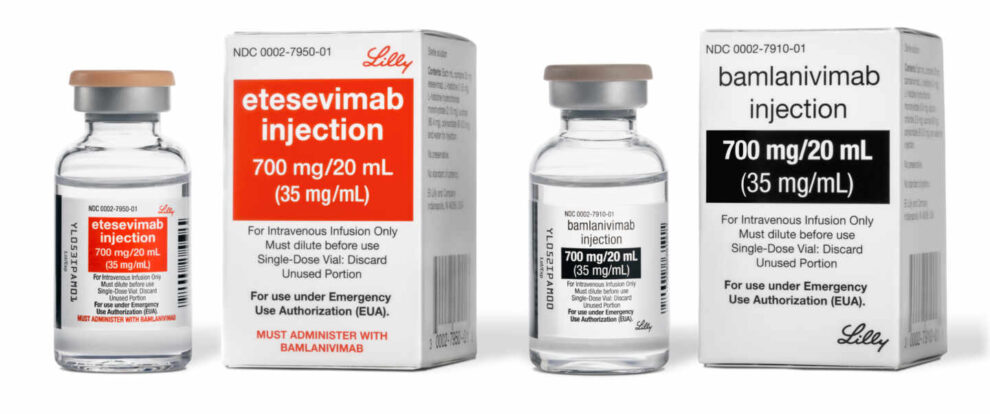
"Lo importante de nuestro tratamiento es que se dirige a pacientes ambulatorios, cuyo estado es leve o moderado y que no están hospitalizados, a diferencia del remdesivir o la dexametasona", explica a El Independiente José Antonio Sacristán, director médico de la farmacéutica Lilly, responsable del desarrollo del fármaco.
Los resultados disponibles de los ensayos en fase 2/3 con bamlanivimab han demostrado reducir un 70% el riesgo de hospitalización, además de reducir los síntomas y la carga viral. Cuando se añadía además etesevimab, se comprobó una reducción del riesgo de hospitalización y muerte por Covid en un 70%. Todos eran pacientes con la enfermedad en fase leve o moderada y no hospitalizados.
¿En qué consiste el tratamiento y cómo se administra?
Los anticuerpos monoclonales son proteínas producidas en laboratorio que imitan la capacidad del sistema inmunológico para combatir los virus. Bamlanivimab es un anticuerpo monoclonal dirigido contra la proteína S (spike) del SARS-CoV-2 con el objetivo de bloquear la adhesión y la entrada del virus en las células humanas.

Etesevimab actúa igualmente contra la proteína S para bloquear la unión del virus al receptor de superficie ACE2 de la célula huésped. Éste se desarrolló a través de la modificación genética de un anticuerpo IgG1 humano nativo y que habían desarrollado Junshi Biosciences y el Instituto de Microbiología - Academia China de Ciencias (IM-CAS). Junshi Biosciences lidera el desarrollo en China, mientras Lilly lidera su desarrollo en el resto del mundo.
Bamlanivimab se administra en una única dosis inyectada durante 15 minutos, según explica Sacristán: "Es una única dosis la que ha demostrado resultados, siempre a pacientes leves no hospitalizados y que tengan un alto riesgo de empeoramiento".
¿Para qué pacientes va dirigido?
Ambos fármacos están indicados para niños desde 12 años y adultos que presenten condiciones de alto riesgo frente al Covid. Entre estas, explica Sacristán, "están las personas mayores de 65 años, las que padecen obesidad, diabetes, enfermedades crónicas o inmunodeficiencias".
El uso del fármaco está indicado a personas que cumplan los criterios de riesgo y que hayan sido diagnosticadas de la infección entre dos y diez días antes del tratamiento.
Precio, coste o beneficio
El precio del tratamiento (una única dosis) se sitúa "en torno a los 1.000 euros para los países desarrollados", según Sacristán. Un elevado coste que corresponde "al desarrollo complejo de este tipo de fármacos" y que goza de una gran relación "coste beneficio en función de los gastos de hospitalización que ha demostrado ahorrar", añade el director médico de Lilly.
Alemania ha sido el primer país de la UE en anunciar compras Bamlanivimab (y otro anticuerpo monoclonal) en 200.000 dosis a finales de enero. Según explica Sacristán, el fármaco ya se ha autorizado de emergencia en Estados Unidos, Canadá, Alemania, Igalia, Italia, Hungría, República Checa, Suecia, Israel y Emiratos Árabes Unidos. La combinación de bamlanivimab y etesevimab ha recibido también una autorización de uso de emergencia en EE. UU. e Italia.
España aún no ha adquirido el fármaco, que tampoco se ha usado en el contexto de los ensayos clínicos, pero Sacristán asegura que las conversaciones de la farmacéutica con la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) está avanzando y que el uso podría llegar "de forma inminente".
La posibilidad de contar con un fármaco para los más vulnerables frente a la enfermedad es uno de los retos para controlar una pandemia que dura ya más de un año y que ha dejado más de 70.000 muertos en España y de 2,6 millones de muertos registrados en el mundo entero.
Te puede interesar
Lo más visto