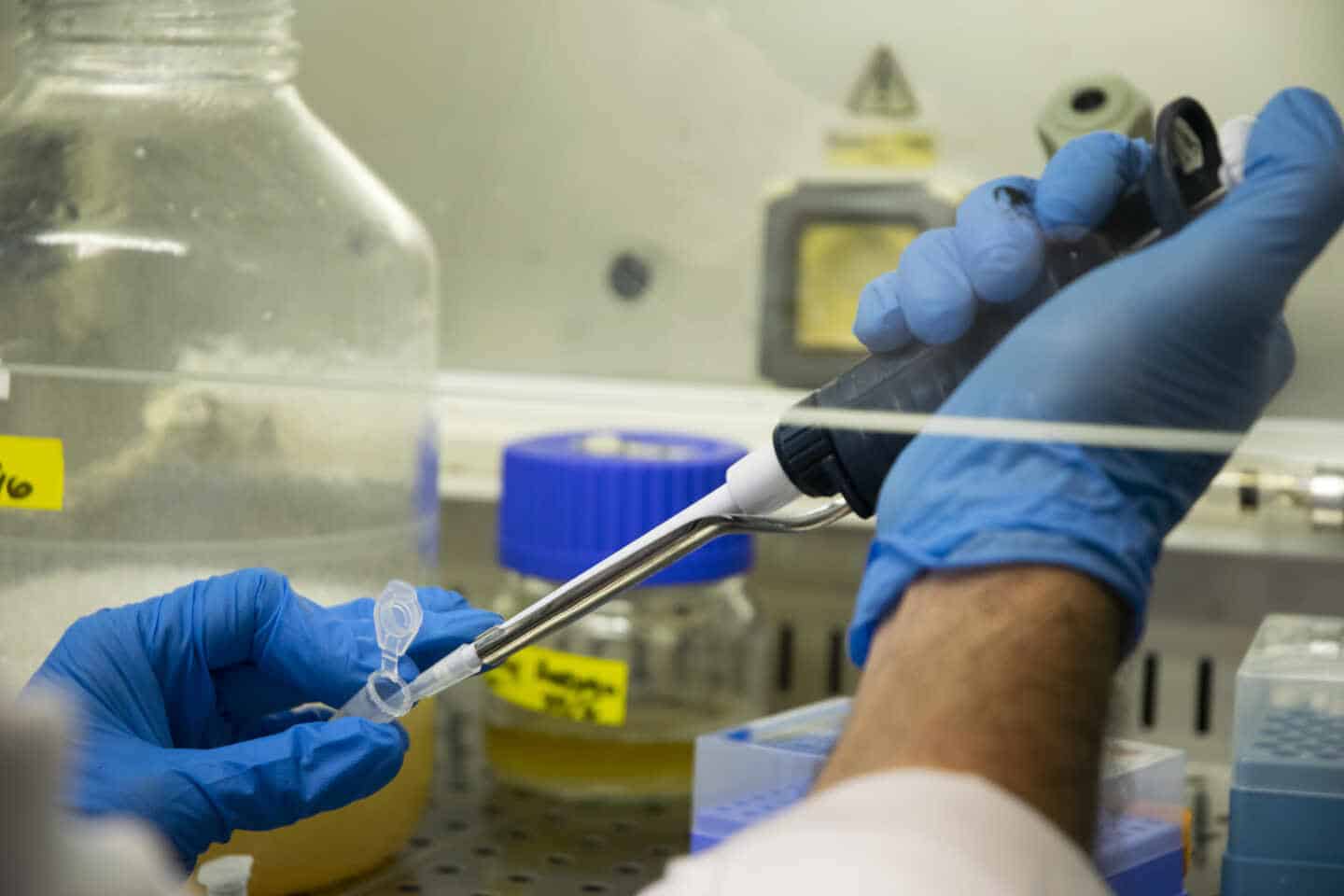
Los test serológicos desarrollados por el Consejo Superior de Investigaciones Científicas (CSIC), con una fiabilidad del 98%, podrán llegar a todo el mundo de forma más igualitaria como la primera tecnología de salud Covid con una licencia "transparente, global y no exclusiva".
Así, la organización española se convierte en la responsable de la primera licencia del C-TAP, la plataforma lanzada por la Organización Mundial de la Salud para facilitar el acceso a las tecnologías de salud en todo el mundo. El acuerdo se firma también con la organización Medicines Patent Pool (MPP), vinculada a Naciones Unidas, para garantizar que los países de ingresos medios y bajos puedan producir y utilizar estos test. En esos territorios, los test se utilizarán sin necesidad de pago de royalties o derechos.
El CSIC se compromete así a ceder a estas organizaciones todo el conocimiento relativo a los test, el material biológico necesario para producirlos y la formación necesaria para que los países puedan ponerlo en marcha. Es la primera vez que se hace, como ha destacado la directora del CSIC, Rosa Menéndez, quien ha asegurado en el acto en que se ha desarrollado la firma del acuerdo que esto es "el inicio" y que la idea es "seguir hablando sobre otras tecnologías en desarrollo en la organización".
Como ha destacado en el acto la subdirectora general para Acceso a Medicamentos, Vacunas y Productos Farmacéuticos de la OMS, Mariangela Simão, el acuerdo "supone un avance simbólico" por ser la primera patente cedida con estas características. También el director de la MPP, Charles Gore, ha calificado esta primera licencia del C-TAP como un "punto de inflexión" y "extremadamente importante como paradigma para las organizaciones que vengan después".
Se trata de la primera licencia del C-TAP para un test serológico y cualquier tecnología C-TAP. Hasta la fecha, también han firmado acuerdos con los dos tratamientos antivirales, aún en desarrollo, de Merck y Pfizer (Molnupiravir y Paxlovid) para un grupo de países.
El objetivo de la licencia, como ha destacado la representante de la OMS, es "facilitar la producción y comercialización del test serológico por todo el mundo". El acto también ha contado con un mensaje en vídeo del director general de la OMS, Adhanom Ghebreyesus, que ha valorado que el acuerdo incluye la ausencia de royalties para los países en vías de desarrollo con la ventaja de que es además "fácil de usar y adecuado para países con pocas infraestructuras de laboratorio".
En qué consisten estos test
Estos test serológicos fueron presentados ya en julio de 2020 en el CSIC y se producen en España desde otoño de 2020 a través de la empresa ubicada en Salamanca Inmunostep. En aquel momento, una de las científicas responsables de los test, Mar Valés, destacó que el reto y el logro del test había partido de la identificación de una proteasa que era capaz de generar gran cantidad de anticuerpos.
Valés y José Miguel Rodríguez, otro de los científicos responsables, explicaron también en un vídeo difundido en diciembre pasado que el test había sido probado en los hospitales madrileños de La Paz y La Princesa.
Otra de las características de estos tests es que señalan la presencia o ausencia de tres tipos de anticuerpos y que es capaz de diferenciar los anticuerpos generados por la infección natural de aquellos producidos tras la vacunación.
El responsable de la estrategia comercial del CSIC, Javier Maira, ha asegurado que los tests están basados en cuatro materiales biológicos que se ceden junto al conocimiento y la formación. El test se desarrolla en dos formatos - test Elisa y tira cromatográfica - ambos que "no requieren grandes inversiones y son fáciles de desarrollar".
Reacciones positivas del tercer sector
Este acuerdo es una "buena noticia" también para una de las organizaciones españolas más implicadas en el acceso equitativo a fármacos y atención sanitaria, la Fundación Salud por Derecho. Su directora, Vanessa López, aduce que "primero, porque España tira del carro de una iniciativa que tiene como objetivo compartir el conocimiento y apostar por la ciencia abierta; y segundo, porque sumarse a C-TAP permitirá aumentar la producción de este diagnóstico en países de medios y bajos ingresos, acabando con la dependencia de estos países y haciendo más fuertes sus sistemas sanitarios.
También ha lanzado un comunicado celebrando el acuerdo Médicos Sin Fronteras, que sin embargo ha añadido que "una licencia de un dueño de una tecnología no es suficiente para abrir una plataforma para todos los desarrolladores de todos los países" y ha apostado por una "eliminación de las barreras de propiedad intelectual en todos los componentes tecnológicos".
Te puede interesar
Lo más visto