En noviembre de 2020 el Gobierno de España celebraba que en 2021 España contaría con "hasta siete vacunas" para combatir el Covid. La Comisión Europea había cerrado entonces preacuerdos de compra con cinco compañías - Pfizer, AstraZeneca, Moderna, Sanofi y Curevac - con el objetivo de disponer de las dosis necesarias en cuanto estas vacunas fuesen autorizadas por la Agencia Española del Medicamento.
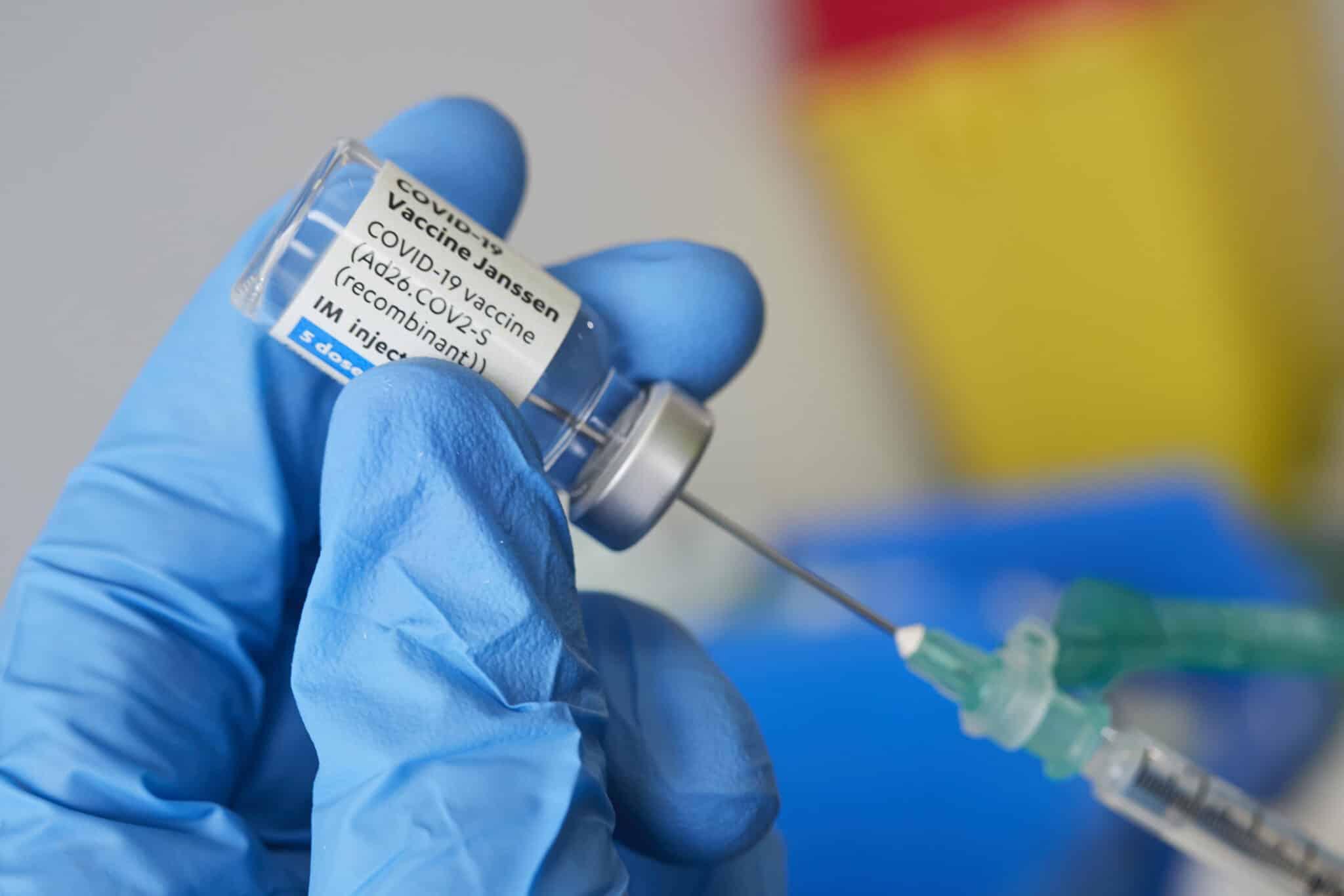
Las expectativas se cumplieron y con pocas semanas de diferencia se autorizaron las vacunas de Pfizer (21 de diciembre de 2020), Moderna (6 de enero de 2021) y AstraZeneca (29 de enero). Después solo se sumaría Janssen, la esperada inyección unidosis (11 de marzo).
Desde entonces y casi siete meses después, la aprobación de vacunas en la Unión Europea se ha estancado, ya que algunas de ellas como las de Novavax y Curevac llevan desde febrero bajo el análisis de Europa, en el llamado proceso de rolling review. También siguen en él la rusa Sputnik desde marzo y la china Sinovac desde mayo. La de Sanofi también está bajo el análisis de la agencia ya desde julio.
Las causas de este estancamiento no están claras, pero en la última comparecencia del Comité de Medicamentos de Uso Humano de la EMA no se habló de ellas sino de tratamientos, como el antiviral de la estadounidense Merck y otros anticuerpos monoclonales.
"Es difícil saber que se ha cocinado en los entresijos de la EMA para no mover con celeridad el rolling review de las vacunas Sputnik, Curevac o Novavax. Espero no se deba a imperativos geopolíticos, nacionalismos vacunales europeos o guerras comerciales que utilizan la regulación sanitaria para proteger mercados de productores europeos o norteamericanos. Me gustaría poder entender por qué se ha ralentizado el proceso, que fue tan rápido los primeros meses", reflexiona al respecto el exdirectivo de la Organización Mundial de la Salud, Daniel López-Acuña.
Algunas de esas vacunas, como la Sputnik, cuentan además con los datos de hasta 70 países donde ya han sido aprobada y llevan meses inoculándola. Una razón que hace que el genetista y experto en Covid de la Universidad británica de Leicester, Salvador Macip, cuestione también este retraso. "No parece que pueda haber un motivo científico sino más bien político, especialmente cuando hablamos de vacunas que han sido aprobadas en otros países", afirma.
No obstante, la OMS también mantiene paralizada la aprobación de Sputnik, que se ha puesto en Rusia, Latinoamérica o Asia entre otros lugares. Hace dos semanas un directivo de la OMS explicó que "es un grupo que trabaja de manera independiente y que informará de sus conclusiones una vez que concluya sus labores" y que éste es un asunto de "semanas o meses", como recogió EFE.
Los resultados de los ensayos presentados por Sputnik hablaban de una efectividad de más del 97%, del 89% en el caso de la estadounidense Novavax.
Lo cierto es que con las cuatro vacunas autorizadas en Europa la Unión ha vacunado ya a tres de cada cuatro europeos y, además, ha ampliado contratos hasta 2022 por una cantidad muy superior a la de los habitantes. "En los primeros meses había mucho interés por conseguir vacunas pero ahora ya no existe el mismo incentivo puesto que ya hay suficientes dosis comprometidas", cree Macip.
En la página del Gobierno de España, no obstante, siguen figurando un total de ocho vacunas de las que se han adquirido o precomprado 251,2 millones de dosis, sin contar las de Curevac, Sanofi y Valneva en las que el número de dosis está "por concretar".
Desde la perspectiva de López-Acuña dos razones pueden ser las que estén provocando este rechazo: "O los dossiers que han presentado los productores de estas vacunas no son suficientemente convincentes porque no cumplen con los requisitos de seguridad y eficacia que requiere una aprobación objetiva de un medicamento o una vacuna, en cuyo caso tendría sentido, o bien se utiliza una ralentización del rolling review para proteger la producción y comercialización de vacunas europeas y norteamericanas y asegurar sus nichos de mercado, en cuyo caso estaríamos hablando de procesos no objetivos de regulación sanitaria al servicio de tácticas comerciales".
El que fuera tres décadas directivo de la OMS denuncia esta postura y afirma que "la EMA debe ser transparente y pronunciarse con claridad al respecto para no sembrar dudas si no están justificadas y para dar a la gente y a los profesionales las certezas que merecemos".
Te puede interesar
Lo más visto