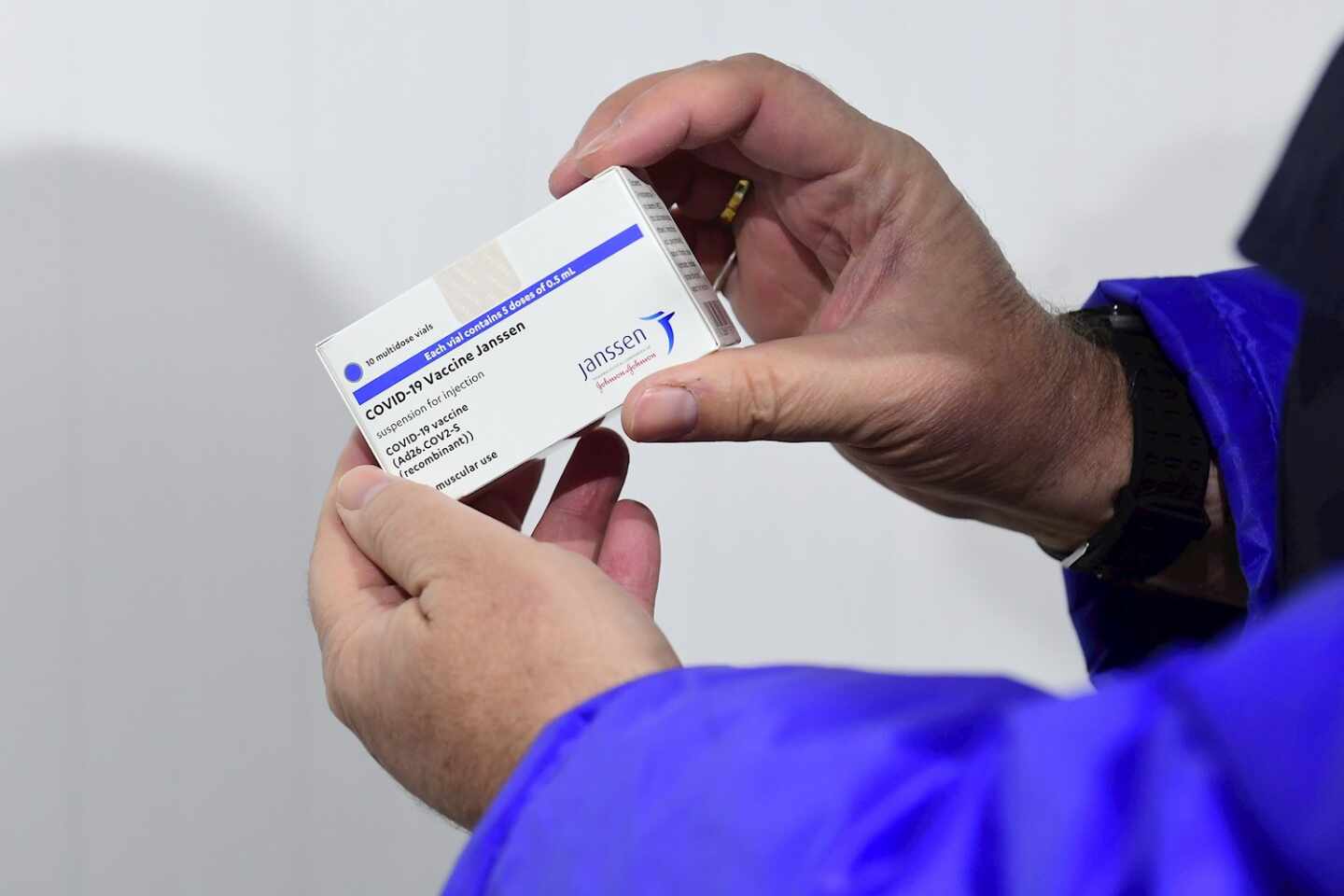
La Agencia Europea del Medicamento (EMA) ha concluido, tras analizar los casos de trombos registrados en personas que habían recibido la vacuna frente al Covid de Janssen, que el "balance riesgo beneficio de la vacuna sigue siendo positivo" y recomienda por tanto la vacunación con este fármaco, que fue autorizado en la Unión Europea el pasado 11 de marzo.
LA EMA afirma que hay un "posible vínculo" entre los "casos inusuales de trombos con bajada de plaquetas en sangre" y la vacuna pero afirman que "el balance riesgo-beneficio de la vacuna sigue siendo positivo". Por tanto, recomienda que la ficha técnica de la vacuna incluya estos eventos como "posibles efectos adversos muy raros".
Justo cuando la cuarta vacuna aprobada para su uso de emergencia en la Unión Europea se empezaba a distribuir en Europa, la agencia reguladora sanitaria estadounidense (FDA) recomendaba paralizar su uso en EEUU. La causa, la detección de ocho trombosis de senos venosos cerebrales entre los cerca de siete millones de vacunados. Los trombos se asociaban también a disminución de plaquetas en sangre y tenían características similares a las asociadas con la vacuna de AstraZeneca.
Ese mismo día, el propio laboratorio afectado anunció que interrumpía la distribución de su vacuna en Europa hasta la resolución de la investigación de los posibles efectos adversos.
En su análisis, la EMA afirma que ha tenido en consideración toda la evidencia disponible, ocho casos de trombos de estas características en EEUU (con una muerte) de entre siete millones de vacunados. Todos los casos ocurrieron en las tres semanas después de la vacunación y se concentraron en mujeres menores de 60 años. Ninguno en personas mayores de esa edad. Destacan que los casos son muy similares a los asociados a la vacuna de AstraZeneca y que no se han podido identificar factores de riesgo específicos de edad o sexo.
Seis síntomas para buscar "atención médica inmediata"
La Agencia Europea del Medicamento explica que aunque son "muy raros", quienes hayan recibido la vacuna de AstraZeneca deben estar atentos durante las tres semanas posteriores a alguno de los siguientes síntomas:
- Dificultad para respirar
- Dolor en el pecho
- Hinchazón en la pierna
- Dolor abdominal persistente
- Síntomas neurológicos como dolor de cabeza fuerte y persistente o visión borrosa
- Pequeñas manchas rojas debajo de la piel en el sitio de la inyección
La directora ejecutiva de la EMA, Emer Cooke, ha incidido en que "la rápida intervención del médico puede cambiar el pronóstico" y también Sabine Straus, la directora del Comité de seguridad de los medicamentos, que ha subrayado que "si se tratan rápido, se pueden evitar complicaciones".
Sobre los tratamientos, Straus ha subrayado que aún no se puede concretar de forma específica pero ya se puede plantear la "no recomendación de heparina y si de inmunoglobulinas para tratar estos problemas de coagulación".
La Agencia Europea del Medicamento ya estaba analizando la relación de las vacunas aprobadas frente al Covid y la posible aparición de trombocitopenia inmune, el trastorno de bajada de plaquetas que se asocia a las trombosis investigadas en relación con las vacunas. Así mismo, también estaba estudiando la aparición de posibles trombos tras la vacunación con Janssen tras la aparición de "alertas de seguridad" antes de la paralización de Estados Unidos.
Straus también ha subrayado que "la principal hipótesis para estos casos es una respuesta inmune similar a la que se relaciona con la vacunación de AstraZeneca y que sucede también como una reacción a la heparina".
El precedente de AstraZeneca
Esta resolución es la segunda que estudia la relación de una vacuna frente al Covid y posibles trombos. La EMA ya informó - y sigue estudiando - la asociación de la vacuna de AstraZeneca y casos de trombosis de senos venosos cerebrales y trombosis esplácnicas (abdominales), asociadas ambas a una bajada de plaquetas.
Del primer estudio en profundidad con el fármaco de AstraZeneca, la EMA concluyó que aunque había una "fuerte asociación" entre el fármaco y los trombos, la vacuna sigue siendo segura y efectiva y recomendó seguir utilizándola. Sin embargo y pese a esa resolución, muchos países decidieron restringir o incluso desechar su uso (como Dinamarca) y otros como España restringieron los grupos etarios a los que ofrecerla, en concreto y de momento solo reciben esta vacuna personas entre 60 y 69 años.
Preguntada por el análisis de la vacuna rusa Sputnik, también basada en adenovirus (como AstraZeneca y Janssen) y que Europa evalúa para su posible aprobación, Cooke ha afirmado que "el análisis es aún preliminar y no se ha mirado aún datos de farmacovigilancia, pero se prestará especial atención a estos posibles eventos".
La restricción de uso de las vacunas autorizadas de adenovirus pone en jaque los planes de vacunación de España y puede suponer un sobrecoste para España de hasta 650 millones de euros.
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha emitido pocos minutos más tarde un comunicado en el que recoge la información aportada por la EMA y que insta a los profesionales sanitarios a vigilar los posibles síntomas de alerta. Se espera ahora que el Ministerio de Sanidad autorice el inicio de la vacunación con este fármaco y determine si habrá restricciones de edad u otro tipo para su administración, en línea con lo ocurrido con AstraZeneca.
Te puede interesar
Lo más visto